一个研究小组通过与德克萨斯大学MD安德森癌症中心的多中心研究,宣布了一种新的胃癌遗传分类系统。本研究可为胃癌的个性化治疗奠定基础。
MD安德森癌症中心、高丽大学医学院、CHA大学医院、庆熙大学医学院、延世大学医学院、成均馆大学医学院等5个机构;参与本多中心研究。
该研究结果发表在《分子癌症》杂志上,由MD安德森癌症中心的李ju - Seog教授主导,肿瘤血液学部的吴尚哲教授参与。外科Sang - Hee Kang教授和消化内科及肝脏内科Sun Young Yim教授作为共同第一作者参与研究。
此前,MD安德森-高丽大学研究组也在《肝病学》上发表了肝癌的遗传分类系统。
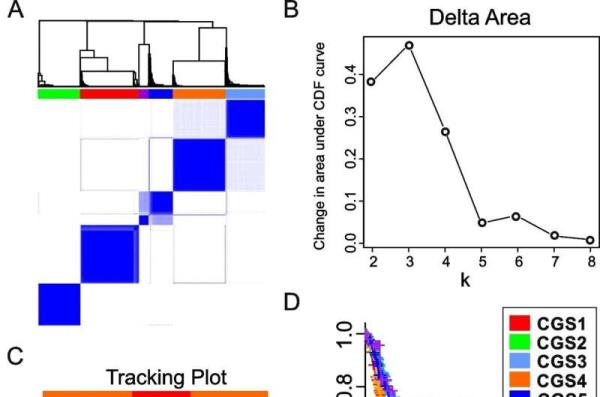
胃癌具有遗传和临床多样性。研究组对过去发表的8种胃癌的基因分类系统进行了分析,得出了6种共识基因组亚型(Consensus Genomic Subtypes, CGSs)的结果。该系统根据不同的基因表达模式将胃癌分为CGS1到CGS6。
每个亚型有不同的特征,CGS1表现出最差的预后特征。它具有非常高的干细胞特性和低基因修饰。然而,分析证实CGS1对免疫治疗反应良好,针对IGF1R的治疗可能有效。CGS2在典型上皮细胞基因表达中富集。CGS3和CGS4克隆数变异大,对免疫治疗反应低。
然而,CGS3具有HER2基因激活的特征,CGS4具有SALL4基因激活的特征。研究小组分析说,针对这些特征的治疗将是有效的。CGS5具有高突变负荷,这是肿瘤微卫星不稳定性的特征,对免疫治疗反应中等。CGS6对感染性单核细胞增多症(Epstein Barr)病毒呈阳性,甲基化水平非常高。它对免疫治疗有很高的反应。
研究小组不仅对胃癌的遗传学进行了分类,而且通过对基因组和蛋白质组数据的系统分析,估计了每个亚型的标准治疗和实验治疗(放化疗、免疫治疗等)的潜在应答率。因此,由于高水平脂质过氧化导致的铁依赖性细胞死亡,CGS3亚型在抗癌放疗中表现出特别大的益处。研究提出了每种亚型的潜在治疗对象。
该研究的主要作者之一,胃肠病学和肝病学部门的孙永严教授说:“尽管由于新疗法的实施,胃癌的死亡率正在下降,但它仍然是癌症患者死亡的主要原因之一。我们相信这项研究将为个性化胃癌治疗奠定基础。”
更多信息:Yun Seong Jeong等,临床保守的胃腺癌基因组亚型,Molecular Cancer(2023)。DOI: 10.1186/s12943-023-01796-w杂志信息:分子癌症,肝病
高丽大学医学院提供
引用:一个新的胃癌基因分类系统(2023,11月6日)检索自https://medicalxpress.com/news/2023-11-gene-classification-gastric-cancer.html
作品受版权保护。除为私人学习或研究目的而进行的任何公平交易外,未经书面许可,不得转载任何部分。的有限公司
内容仅供参考之用。



